���F�ڵ�λ�ã� �ٝ�����ˎ���W��� >> �β��� >> ��ˎ�ӑB
�������������ײ�����Ⱦ̎������Ԕ����B
- ��Դ�� ����ˎ��ˎӍ ���ߣ��ٝ��ӑB �g�[�� �l���r�g��2006/9/9 18:00:00
��������������������Ⱦ̎������Ԕ����B
�ژ��� ������ ꐳɂ� �ݸ��� Ҧ����
���������ף�CHB����������ȫ����Ҫ�Ĺ����������}����s25%���׃��r�ڸ�ȾHBV�Ļ�������Ӳ�����ΰ����^���������������β��W�ҽM�ɵČ���С�M��ǰ����ӆ�ͳ������P��CHB��̎�����̡��b�ڌ�CHB���J�R�������F�еĸ������еķ�������W�\����Ľ��������ί��ֶεij��F�Լ����@�ʵ��ί������ĸ��N��ȱ�c�J�R�ļ����ԭ�е��ί����M����ӆ�ı�Ҫ����ӆ��ϵ�y�����īI���@�C������A�������ڲ���ȱ�����w�����Y�ϵă��ݣ����ҽM��Ҫ�����R�����͌��ҹ��R�M����ӆ��Ŀǰ���������з�������W�������ѿəz�y����10 IU/ml��Ѫ��HBV DNA������R�����_���������ί�ǰ���ߵĻ���HBV DNAˮƽ���O�y���������ί��đ���ͱOҕ������ˎ�����ˎ��r���������ί�����ҪĿ���dz־�����HBV���ƣ��M����ʹѪ���е�HBV DNA�������ˮƽ���P���m�Ͽ������ί���HBV DNA�ֵHBeAg��Ե�CHB���ߞ��20000IU/ml�� HBeAg��Ե�CHB�����˽��͞��2000IU/ml��ʧ�����Ը�Ӳ�����ߞ��200 IU/ ml���ɔ_�ئ�-2b�����������¸��f�����濨�f�����Ҷ������ɔ_�أ�PEG-IFN) ��-2a�Ⱦ��ѱ���������CHB���ߵij�ʼ�ί������������ס��x��r��Ҫ���]�Ć��}������Ч����ȫ�ԡ���ˎ���ʡ��oˎ�������ί��M�õȡ�
���������ײ�����HBV��̎�������������β��W�ҽM�ɵČ���С�M��ӆ�����һ����2004��l�У��˺����ЃɷNˎ������濨�f����Ʒ����·�������a�̞�ٕr��ʩ�F����˾���;��Ҷ������ɔ_�ئ�-2a(��Ʒ�����_�������a�̞��_�Ϲ�˾��������ʳƷˎƷ�O�������֣�FDA�����������ί�CHB�����ڌ�CHB��Ȼʷ�����J�R�����к�@�õ�ˎ���u�r�Y�ϣ����ҽM�ɆT�ٴξە��������u�r����ӆ�ί����h����Ŀ���nj���ǰ��ӆ�����P��������HBV��Ⱦ���\�ࡢ�ί��ͱO�صČ��þC���������Mһ�����a����ӆ���������B�m���īI������structured literature review�����͌��F���ί�ָ�ϵ��u�������Ը�λ���ҵĪ����{���о�����A�����ҽM���³��F���Y���M������e���Ա�C���u�����B�m���īI�����Ĵ�ʩ������PubMed����īI�������ЏV���z��2003��1��1����2005��7��28��֮�g��������PCHB�ί���Ӣ��Փ�ġ����⣬�������PՓ���M�е��ֹ��īI�z���Լ����I��֮�g�Ĵ���Ҳ�鱾�����̵���ӆ�����˅����Y�ϡ�ͨ�^��ӆ���_�IJ��ú��ų��˜ʌ�ijһ�īI�Ŀɽ��ܶ��M���u��������455���īI�вɼ{��37��Փ�ġ�����߀��2004��2005������������ܣ�Digestive Disease Week��DDW����2003��2004��������β��W����American Association for the Study of Liver Diseases��AASLD�������2004��2005��ĚW���K�о��f����European Association for the Study of the Liver��EASL�����Փ�ļ����xȡ28ƪժҪ�����������˺�߀��2005��AASLD������xȡһЩժҪ�����a����
�ڱ��Ε��h֮ǰ�����ҽM�ɆT�������������c�P�I�Q�h�c�������ľC���R����r�²�ͬ�ί��x헵�ǡ�����M�����u����һ�N9�����u���������Á�ͻ���@ʾ�����P�ί��x�ǡ������һ�»������Ҋ���@�N�u����Ϣ���Á�̽�����N������Ҋ���ڵ�ԭ���Ԏ������ҽM�_�ɹ��R��ֻҪ�п��ܣ����ҽM����ѭ�C�t�W�C��������h�������ȱ�����������C�Y�ϣ����ҽM�ɆT�������������˵��R���������P������Ҋ�������h���������̡���Ŀ���ǎ��������t���ش����P���H���}��������Ҫ���ηN�z�飬��ν�ጙz�Y������Щ������Ҫ�ί����Εr�_ʼ�ί����ί����L�r�g������Щ���е��ί��x헣��Լ���αO�y���ߵIJ���ȡ����_���@Щ���]��Ҋ�r����δ���]�ί��M�Æ��}�����Ŀǰ��ȱ��ᘌ��������������ί�CHB��ijɱ�-Ч���Y��
һ������ؓ��
����Ӌ��ȫ����������3��5�|����HBV��Ⱦ�ߡ��mȻ����HBV��Ⱦ��������r�����S���������ң�����ӋҲ��125�f�˸�ȾHBV��Ȼ����������CHB������r�п��ܱ���������������������ā��ޡ��Ж|�����ȵ������M����������Ⱥ�У�HBV��Ⱦ��������r��5%һ15%���ȣ���ӳ������ԭ������ס���ҵ�HBV��Ⱦ������ģʽ�����^ȥ��10���У����������˔��������@�����L������ӋĿǰ���мs105�f�ˡ�����������������ͳ����M�е�һ헙M�����{���@ʾ�������Ї����n����Խ�ϵ���Ⱥ�У�HBsAg��Ѫ��W�����ʞ�10.4%���ڼ~�s���M�е�һ헻�����{���@ʾ���~�s�ā����������У��əz��Ѫ��HBsAg�߸��_�@�˵�23%��1990һ2002���g���������İl���ʽ�����67%������ԭ�����ڏV���ӷN���������硣�M����ˣ��°lHBV��Ⱦ��Ȼ���^��Ҋ�����������������c�A�����Ĺ�Ӌ��������ÿ��s��7�f�˰l������HBV��Ⱦ��CHB���߰l����Ӳ�����ι���ʧ�������μ�������HCC�����L�U���ӡ�����Ӌ����s25%���׃��r�ڸ�ȾHBV�Ļ������Ӳ����ΰ����^����������Ӌ�����������@ЩHBV��Ⱦ���P���l�Y�Ļ���ÿ����_5000�ˡ�
������Ȼʷ�����P�g�Z
�l������HBV��Ⱦ��s3%һ5���ij��˺�95%�ă�ͯ���߲��ܮa����ֵ����ߑ��������HBV��Ⱦ���@Щ���ߌ��lչ������HBV��Ⱦ�����������l���о�Ժ��NIH�����������M�����õ���������HBV��Ⱦ��ͬ�A�ε��R���g�Z�����\���˜ʿ��Y�ڱ�1�������cHBV��Ⱦ���P���R���g�Z���Y�ڱ�2��

ժ���ԣ�Lok and McMahon��a������λ�z�˱��ĽM���W���F��b���^������@�����ǰC��C�����ӵ�ͻ׃��c������PCR���п��ܜy���O�͵�HBV DNAˮƽ

ժ���ԣ�Lok and McMahon
����HBV��Ⱦ�Ę�־��Ѫ���г��m����HBsAg��HBeAg����ˮƽHBV DNA�����˫@����HBV��Ⱦ�������A�γ��������@�IJ����Ӻ�ALTˮƽ���ߣ������a�ګ@�ø�Ⱦ�ߵ�ALTˮƽ��څ�����������������A�Σ���������һ����r��Ҳ���Ի�Ӳ���ALTˮƽ���ߣ���ͨ���ڳ�����֮ǰ�������F��HBeAgѪ��W�D�Q����Ȼ�l����Ҳ���ڿ������ί���l������ALTˮƽ������r�³�Ҋ����HBeAg��ʧ��Ѫ��W�D�Q֮ǰ��ͨ�������@��Ѫ��HBV DNAˮƽ�½���<20000IU/ml������ͨ������ALTˮƽ�ͳ�����ˣ�HBeAgѪ��W�D�Qͨ����ʾ��CHB�D��ǻ����HBeAg�y����B�����ߛ]�����@���R�������C����Ѫ��HBV DNA̎�ڸ��͵�ˮƽ�����ֻ���HBsAgҲ��ʧ�����@��������HBV��Ⱦ�Ŀ���resolution����Ȼ����һ����r�½^�����CHB���ߵIJ�����Եõ����ƣ��������ܸ���������
һ���ְl��HBeAgѪ��W�D�Q�Ļ��߿��Գ��FHBV DNAˮƽ���ٶ����ߣ��Լ�ALTˮƽ�ij��m���gЪ�����ߡ��@����w������Ȼ�l����HBV׃���꣬�Ķ����������{��HBeAg�Įa������C��ͨ��������ǰC��C�����Ӆ^�l����׃�����@�N��͵�����HBV��Ⱦ���Q��HBeAg��-����CHB����ˣ�CHB���Է֞�ɷN��Ҫ����ʽ��HBeAg��+����CHB��HBeAg��-����CHB ��һ헌�283���l����ȻHBeAgѪ��W�D�Q�Ļ��ߵ��о��@ʾ����ƽ���S�L�u��8��6���s2/3�Ļ��ߞ���mHBeAgѪ��W�D�Q��24%�Ļ�����ALT�����ߣ��c�z�y��HBV DNA���P��
�β���ӵ��l�l����spontaneous flares��������CHB����Ȼ�^���аl�������Ͱl������ӄ��Ɍ����Mչ�Ը��w�S����Ӳ�����������°��������Ƶ�HBV DNA���d����ALT��������r�£�����HBV���Ը�Ⱦ��һ�N�Y�����λ�z�l�F���g�^���ߵĸ��w�S���ܿ��ܱ����g�^�p�Ļ��߇��ء������o���ί�������HBV DNA��ALTˮƽ���ߵ�HBeAg��+����HBeAg��-��CHB�Mչ���Ӳ���ı����ܸߡ���2헰�ο�������о��ĸλ�z�Y���@ʾ��δ���ί��Ļ�����48���Ժ��Mչ����w�S���ı������_21��һ36%������CHB���ߣ����д����Ը�Ӳ���ߵ�5�겡���ʞ�16%������ʧ�����Ը�Ӳ���Ļ��ߣ�������M������ֲ���t5�겡���ʞ�65��һ86%��HBeAg��HBV DNA�Ĵ���ʹ�l��HCC���L�U���ӡ����о��@ʾ���c�oHBsAg�����HBsAg��HBeAgͬ�r��Ե����Ի��ߣ������㣬���Mչ��HCC������Σ�U�Ȟ�60.2������HHBsAg��ԣ��t����Σ�U�Ȟ�9.6)��ԓ��о�߀��ʾ���܉�y��HBV DNA����֦�DNA������Quantiplexԇ���У�Chiron��˾���Ļ��ߣ���l��HCC�Ŀ����Ԟ鲻�ܜy��HBV DNA�ߵ�3 .9������HBV DNAˮƽԽ�ߣ��l��HCC���L�U��Խ��
�½��l����һ헌�3 653��CHB���ߣ�����164�����߰l����HCC�����L������о��l�F��HCC�İl�����cHBV DNA�������ݶ����P���༴�cHBV DNAˮƽ֮�g�ʬF���Ч����dose-response���Pϵ����HBV DNA��300��ؐ��ml�Ļ��ߣ�HCC���۷e�l���ʞ�1.3%������HBV DNA106��ؐ/ml�Ļ��ߣ�HCC���۷e�l����������14.9%����ȥ�������g���Ԅe���������ƾ����ġ�ALTˮƽ��HBeAg��B�ȶ�N���ص�Ӱ푺�HBV DNAˮƽ�cHCC�l����֮�g���@�N����W�ݶ�Ч����ʮ���@��������һ����Ƶ��о���3 582�������M�����{�飬�@ʾ��HBV DNA��300��ؐ/ml�͡�106��ؐ��ml�ăɽM�����У���Ӳ�����۷e�l���ʏ�4.5%����36.2%���@�NѪ��HBV DNAˮƽ��Ӳ���l����֮�g�����P�Pϵ������HBeAg��B��ALTˮƽ������׃��֮�⡣
����HBeAg��HBV DNA����HBV���ƵĘ�־�����ǰ�����P�о�����ʾ������HBV��Ⱦ�M���д��ڲ������ƣ��@��ͨ�^�������ί�����ֹ�β����Mչ�ṩ�˺���������
��������׃��
HBV��׃���ʴ�s������DNA������10�����c�����^������ۺ�ø��������D�øȱ���^��Ҋ��У�x���ܡ�׃�����l����HBV�IJ�ͬ����Ƭ�Σ����N����׃�������Ȼ���ڿ������ί��x�����°l�����ڮ�ǰ���R�����`�У���4�NHBV��ʽ�����P�ģ�Ұ����HBV��ǰC׃���ꡢC�^������׃���꼰�������ί��T���ĸ��N׃���ꡣ
��һ��ǰC��C������׃���� HBeAgһ�㱻������HBV���ƵĘ�־������HBeAg��-�����J���ǟo�������Ƶ�HBV��Ⱦ��ALTˮƽ������HBV��Ⱦ���������Q�顰�����y���ߡ������F�ڸķQ�顰�ǻ����HBsAg�y���ߡ��������u�r������������������أ���ALTˮƽ���ߵ�ȱ��HBeAg��HBV��Ⱦ�����M�����S���о���20���o80������ڣ��ڵ��к��^�l�FԽ��Խ���HBeAg��-���Ļ����HBV���ƻ��ߡ�1989�꣬���л����HBV���ƵĻ����w�ȷ��x��HBV����M�аl�F������ֹHBeAg�γɵ�����׃�����Ҋ�Ğ�ǰC�^G1896A���׃���������γ�һ�Kֹ�ܴa�ӣ���ֹ��HBeAg�ĺϳɣ��������걻�����顰ǰC׃���ꡱ�������һ�N��Ҫ���p׃������������C�^�������p׃���ꡱ������A 1762T��G1764A�ɷN���׃��������HBeAg�a�����{��
�M���Ј����ǰC׃������l��������HBeAg��-����CHB���ǵ��͵ī@����HBV�¸�Ⱦ��ǰC׃�����������͵�
Ұ����HBV�����Ⱦ�^���еă����꣬����������A��(HBeAgѪ��W�D�Q�����ԺY�x������HBeAg��-��CHB���γɿ�����HBeAgѪ��W�D�Q�ã�Ҳ�����ںܶ���������ʮ����γɡ�HBeAg��-����CHB��2�N��Ҫ�ļ������ģʽ����s30��һ40%�Ļ��߱��F��ALTˮƽ���m���ߣ�����3-4��������45��һ65%�Ļ��߱��F��ALT�gЪ���߲����м��l����Ѫ��HBV DNAˮƽҲڅ�����ߣ��e����ALT����֮ǰ��Ȼ����HBeAg��-��CHB��ƽ��HBV DNAˮƽ����HBeAg(+)��CHB�����m���l�Ծ�����HBeAg��-����CHB�Dz���Ҋ�ģ��H��6%һ15�������L���A��Ҳ����HBeAg��+����CHB���ߣ��䲿��ԭ�������HBeAg(-)��CHB���߶���HBV��Ⱦ���ڡ�
�������������ί��T����׃���� YMDD׃���ǰl����HBVP���a��DNA�ۺ�ø����λ�c���Ұ���-������-�춬����-�춬���ᣨ���Q��YMDD������һ�N����׃�����@�N׃������L-���������ˎ������Ͷ������I���x���ԉ������γɵģ������®a��һ�N����λ�c�l����׃�IJ����ۺ�ø���Ķ���ijЩ�ض��Ŀ�����ˎ��a����ˎ��
�½��ѷ��x��HBV���D�ø���c���¸��f�Ͷ��濨�f���P������׃�������¸��f��ˎ��������HBV���D�ø��B��D�^���FA181V/T�ͣ���N236T�ɷN�P�I׃�����mȻĿǰ��δ�ڑ��ö��濨�f�M�г�ʼ�ί��Ļ������^�쵽��ˎ�C���������ѽ�����������ˎ׃����I169, T184, S202, M250���Ļ����аl�F�ˌ����濨�f�ı�����ˎ��
�ġ�HBV������
����HBV S�����������4%���ϻ�ȫ����M�������8�����ϣ�Ŀǰ�Ɍ�HBV���֞�AһH��8�N�����ͣ�����ȫ��ĵ����ֲ�������ͬ��������A��ҪҊ�ڱ��������W��ӡ�ȼ����ޣ�������B��C��ҪҊ�ځ��ޣ�������D��ҪҊ���ϚW���Ж|��ӡ�ȣ�������E��ҪҊ�����Ǻ��Ϸǣ�������F��ҪҊ���������в����ޣ�������G��ҪҊ�������͚W�ޡ�������H�½����в����������������၆�ݵĻ����з��x��HBeAg��-����HBV��ǰC׃���꣩�Ҋ�ڻ�����B��C��D���@���Խ�ጞ��HBVǰC׃�����Ⱦ�Ҋ�ځ����ϚW��
�����Y���@ʾ��HBV�����Ϳ��ܺ��R��������P������һЩ�о���ʾ���^֮������B��������C�c���β���HCC���Pϵ�������С��c������C��ȣ����^�p�����g�λ�����B�Ƹ��װl��HBeAgѪ��W�D�Q���Пo�Y���@ʾHBV�����Ϳɳ��mӰ푿ڷ����գ��ᣩ�������ί�Ч���������Y���@ʾ��HBV�����Ϳ�Ӱ푌��ɔ_�أ�IFN���đ�����������A��B�c������D��C��ȿ����������ګ@���^�ߵČ�IFN��-2b�Ŀ��������𡣴��⣬�Ј���Q��HBV������A��PEG-IFN��-2a�ί����������^�ߵ�HBeAgѪ��W�D�Q�ʣ�������A��B�ڑ���PEG-IFN��-2b�ί����������^�ߵ�HBeAg��ʧ�ʡ�
�b���@Щ�³��F���Y�ϣ��҂����h���������߳�Ҏ�M��HBV�����͙z�y���Ԏ����Д���Щ���߾��м����Mչ�ĸ��L�U���e����Щ�������m�ϑ���PEG-IFN�ί�����Ӱ푿������ί��Ŀ������ػ�����J�R�����M�ˌ��x��PEG-IFN߀�ǿڷ��������ˎ���M�п������ί��ďV��ӑՓ��Ŀǰ�����P���Ռ�����яV���ṩHBV�����͙z�y���̘I�����ա�
�塢HBV��Ⱦ���\��ָ��
����HBV��Ⱦ���\��ָ����Ҫ����Ѫ����HBVѪ��W�Ͳ����Wָ�˵ęz�y���Լ���ӳ���K��׃��B��Ѫ�������W�ͽM���Wָ�˵ęz�y��
��һ��Ѫ��Wָ�� HBsAg��HBV��Ⱦ�����ȳ��F��Ѫ��W��־���HBsAg���w�ȳ��m����6�������ϣ���ʾ��������HBV��Ⱦ����-HBs�ij��F��ʾHBV��Ⱦ�֏ͺͣ���HBV�a�����ߡ��ڽӷN�����������Ҳ�ɳ��F��-HBs��ż����������HBV��Ⱦ���w�ȿ�ͬ�r�z�y����-HBs��HBsAg����Ŀǰ�������x�в������HBeAg�Ĵ�����ʾHBV���ƻ��S����HBeAg��ʧ������ζ��������ȱ�磬�����HBeAg��-����HBV��Ⱦ��ǰC��C������׃�����r�����ܜy��HBeAg����-HBe�Ĵ��ڳ���ʾ�l����HBeAgѪ��W�D�Q���M����Ҳ���Գ��F��ǰC��C������׃����HBV��Ⱦ��HBeAg��+�����ߵ�Ѫ��W�D�Q��HBeAg��ʧ���y����-HBe�����������ǿ������ί��ĽK�c��������Y���@ʾ�@�N��rͨ���c�����Mչ���L�U�������P�����@�����ܱ��o�����Ժlչ��HCC��
�����������Wָ�� Ѫ��HBV DNA�d����ӳ�˲������Ƶ�ˮƽ���������÷ǔU�����s���������z�yѪ��HBV DNA�����@�N�������������ޣ������z�y�������_105һ106��ؐ��ml����˲����^�m��������HBV��Ⱦ�ߵij�Ҏ�O�y����������NIH���������M���]�������÷ǔU�����s���������܉�y��HBV DNA���༴HBV DNA��105��ؐ/ml(20 000 IU/ml���������o�迹�����ί���Ȼ��������HBeAg���������S��HBeAg��һ���Ļ��ߣ����w�ȵ�HBV DNA���в����ԣ��Еr�ɽ���105��ؐ/ml���¡����ң�Ŀǰ��������c�Mչ�Ըβ����P��HBV DNA�R��ֵ�����Ƕ��١��������ҽM�ɆT�Ľ���ʹ����Ѫ��HBV DNAˮƽ���m��20 000 IU/ml��Ҳ���ܴ����Mչ�Ըβ�����ˣ�HBV DNA��ˮƽ���R�����x�����_���������M�Ђ��Ի�������
�����HBV DNA�z�y�����������о��Դ�����W�����Ķ��������������S����ͺ���߲�����ȕr���܌�����Ѫ�Y�M���u����Ŀǰ��Roche COBAS Taqman HBV DNA����ϵ�y���Ю�ǰ�����_������͙z�y������V�ľ��Զ�����������50һ109��ؐ/ml�������r�ۺ�ø�ʽ������PCR���������đ�����Խ��Խ�V�����ڌ������M�г�ʼ�����u���r�������x�ã��e��Ҫ���nj����ܺ�δ���ܿ������ί��Ļ����M�бO�y��Ŀǰ���ڲ�ͬ�ıO�y����֮�g��ȱ���˜ʻ�������y�Ԍ���ͬ�����֮�g�Ĕ����M�б��^���@һ���}����ͨ�^����һ�N�˜�HBV DNA�����z�y�������Խ�Q�����������еĽY����������IU/ml���λ�M�Ј�棨1 IU/ml�s�ஔ��5.6��ؐ��ml����
�����������W��־ Ѫ��ALTˮƽ�����Ǵ��ڸνM���������װY��ӵĘ�־֮һ����ˣ�ALTˮƽ����һ�㱻�J���Aʾ���Γp��̎�ڽM���W�oֹ�ڡ�ALTˮƽ���m������HBV��Ⱦ�ߣ���λ�z�˱����װY��r���^ALTˮƽ�����ߞ��p������ALTˮƽ������HBV��Ⱦ�ߌ��������ί���Ѫ��W�����������һ���J�鲻�˽o�迹�����ί���Ȼ�����λ�z�@ʾһ����ALTˮƽ������HBV DNAˮƽ�^�ߵĻ��ߴ_�������@���ĸ��K�װY���w�S�����½���3ƪ��������@ʾ��12%һ43%ALTˮƽ���m����������HBV��Ⱦ�ߴ���2�ڻ�2�����ϸ��w�S��������2ƪ�����ʾ�����g����40һ45�q���A�y�@���νM���W��׃�Ī������ء��C�϶��ԣ��@Щ�о���ʾ�������g����40һ45�q��ALTˮƽ����������HBV��Ⱦ�ߵ�̎��ԭ�t�����������e�O�ĸλ�z�����12��һ43�����@��ߴ���2�ڻ�2�����ϸ��w�S�����@Щ���߿�����Ҫ�������ί���
���S���о��C����ALTˮƽ����������ֵ���ܱ��߹������ALT����������������ӆ���ܰ�����һ���ց��R���β����ߡ���һ헴��ͻ�����о�������һ�M���״ΫIѪ����Ҫ�Y��β�����Ⱥ���@��о����@�õ�Ѫ��ALT�������������Ԟ�30IU/L��Ů�Ԟ�19 IU/L���@��������ǰ�������Ę˜ʡ����ң�һ헰���95533�����Ժ�47522��Ů�ԣ����g��35һ59�q����ǰհ������о��@ʾ��ALTˮƽ���˜ʌ����p�����ߵ����ڂ��y�������������ȵĻ��ߣ���β�����������Σ�U���^�ߡ��cALTˮƽ��20 IU/L�Ă��w��ȣ�ALTˮƽ��20һ29 IU/L֮�g�Ļ��ߣ��䲡������Σ�U�ȸ�2��9����ALTˮƽ��30һ39 IU/L֮�g�Ļ��ߣ��䲡������Σ�U�ȸ�9��5������ˣ��{��С�M���h���ڛQ���Ƿ��_ʼ�������ί��r����ALTˮƽ����������ֵ���Զ���30 IU/L��Ů�Զ���19 IU/L��
���ģ��M���Wָ�� ���λ�z�˱��ĽM���W�u�����^Ѫ��ALTˮƽ�������к͜ʴ_�ĸβ���־�����_ʼ�������ί�֮ǰ�����νM���W�Ļ�����B�M���u�������ų�����ԭ������ĸβ��Ƿdz����õġ�Ȼ�����λ�z�����܉���ʹ�õ��\���ֶΡ������䎧�������ԣ���˲��ֻ��ߕ��ܽ^�M�иλ�z��������������w�S����������Ѫ��W��־����о�ȡ�����@���Mչ���mȻ�@Щ�Y�����˹��裬���@Щ������δ�õ�ȫ����C������в����M���R����Ҏ���á�
���������u��

��3���Y������HBV��Ⱦ���ڳ�ʼ�u���r�����M�еęz���Ŀ�������h�������]�o�迹�����ί��Ļ����M���S�L�u������ʼ�u����������ȫ��IJ�ʷ���w��z�飬�eע��HBV��Ⱦ�ΰ�����ʷ���c��������ͬ�r��Ⱦ��Σ�U�����Լ��ƾ�����õȡ�����ҙz���Ŀ�������������β���B���u����HBV���Ƙ�־�HBV�����ͣ�������������Ⱦ�L�U�Ļ��ߣ�Ҳ�茦ͬ�r��Ⱦ�����������M�Йz�y������ALT���m���gЪ���ߵĻ��ߣ����]�M�иλ�z�������ɏ����M�С�����HCC���L�U�Ļ��ߣ����Y��HCC����������������Ҹ棬������ע���A��HBV��Ⱦ�Ă�������H�ͼ�ͥ���н��|�ߑ��M���A���ӷN����Ҏ���߲�Ҫ�^��ƣ����Ҹ��������������܉�õ��C�������^�ƾ���õİ�ȫˮƽ�������и�Ӳ���Ļ��ߣ����h���ơ�����δ�������ײ�����HAV���a�����ߵ�����HBV��Ⱦ�ߣ��������������ƺ��A�����ĵĽ��h�M������ӷN������������2����������ʼע��1�Σ���6��18���¼ӏ�ע��1�Σ���
��һ���μ������ĺY�� HBV�y���߰l��HCC���L�U���ӡ��ڽ^��������ߣ�HCC��������а�Ĥ�Ć��[����ʽ���F���䱶���r�g��2-12���²��ȣ�ƽ��4���£���ͨ�^�����M�м�̥���ף�AFP)�ͳ���(US)�z�飬�������ڰl�FHCC���քe����AFT��US��HBV��Ⱦ���M�ж��ںY�飬��HCC�����аl�FС�ΰ�����5 cm���Ď��ʷքe�s��64%��83%���ϑ���AFP��US�M�Йz�飬���چΪ�������������һ�N�������Y���@ʾ��ÿ6�����M��1��AFP��US�z�飬�^֮ÿ���M��1�Ιz�飬�ܸ���Ч�ذl�FHCC����ÿ3���º�ÿ6���z��1�Σ��ڰl�FHCC��Ч�ʷ���]�����@���
�Y��HCC�Ę˜ʷ�����AASLD���`ָ�Ϻ�EASL���Rָ���о��и�Ҫ�����������½��M������ӆ���������аl��HCC���L�U��HBV�y�����M�кY�顣�@Щ���L�U���߰������^40�q�ā������Ի��ߣ����^50�q�ā���Ů�Ի��ߣ����^20�q�ķ����ߣ���Ӳ�����ߣ���HCC����ʷ�Ļ��ߣ�HBV DNAˮƽ�^�ߵĻ��ߺͣ����и��K�װY��ӵĻ��ߡ����ړ��Ɯy�ڳ����r���׃��r�ڼ��Ѹ�ȾHBV�ā����ߣ��S���R���t�����]�ڸ����ڣ�30һ35�q������p���M��HCC�Y�顣��������J�R������Ҫ��r�ǣ����������ߣ�HCC�����ڟo��Ӳ������r�°l��������ÿ6�����M��1��AFP��US�Y�顣�Ź������z�飨MRI����Ӌ��C���Ӓ��裨CT���r���^�F����һ���J��������HCC���\�������Ը���US������R���t�����h��ijЩ���ߣ��������Ӳ������ֶ�ʹUS��HCC���\�������Ժ͕ܵr������MRI��CT�M�кY�顣�mȻAFP���\�������Ժ͕ܵr������MRI��CT�M�кY�顣�mȻAFP���\�������Բ���US�����кܸߵ�����A�yֵ��99%���������]��HBV��Ⱦ�ط����Ѕ^��HCC��Σ��Ⱥ�M��HCC���ںY�顣
�ߡ��������ί�����
�mȻ������HBV��Ⱦ���ڳ�ʼ�u�r�r�����M�Йz�y��ָ�ˣ�Ҋ��3)���ձ�һ�µ��J�R��������Α����@Щ�z�yָ�ˁ��b�e�������ί����ߣ�ijЩ���}�д��ڠ�Փ��
��һ��ALTˮƽ������������ ALTˮƽ���u�r�β���r��ָ��֮һ�����_����Щ���ߑ����鿹�����ί����������Ҫ���x��Ȼ������ALTˮƽ��������Y�x�������ί�����ı�ǰ��l����������ԡ��μ��������ij̶Ⱥ�ALT ˮƽ���߲��ǿ������P���H�H�z�yALT�����y�������Y�x���иνM���������װY����w�S���Ļ��ߣ��@�c��������r���ơ����⣬ALT�Ļ��Կ����c�w��ָ����BMI�����Ԅe��������֬�|��̼ˮ��������x���Լ������Ƿ�������ί������ت������P�����ߣ�ALT���߿ɳ��F�ڶ�N��ͬ����r�������l��HBeAg��ʧ��ijЩ�������ί���������������Ⱦ�r��
ALTˮƽ���������Q������ҪӰ푣��������Á��A�y������IFN, PEG-IFN��-2a�����¸��f��Ѫ��W����HBeAg��ʧ��Ѫ��W�D�Q����ALTˮƽ���������ί�������A�y�rֵ�ɏ������F�����Mһ���õ��C�����mȻ�����ߌ��������ί��đ����ձ��^�ͣ���ALTˮƽ���ߵĻ��ߌ�����IFN�đ����r�cͬ�Ȳ���ĸ����˷N���ơ�
��ͬ�ĵ�����Դ��HBV������ҲӰ�ALT���鿹�����Q�����ص�Ч���ԡ��^�����������ALTˮƽ������������1/3�Ļ����CHB�������꼴�@��HBV��Ⱦ�ā��������^�Ļ��ߣ�����HBV��Ⱦ�����������A�Ϋ@���\�࣬���A�ε������ǸνM��ȱ���������װY��ӣ�ALTˮƽ��������HBV���ƻ��S���ځ��������^�����аl�F��HBV������B��C�װlչ��HBeAg��-����׃���꣨ǰC��C������׃���꣩���@Щ���߱M�ܴ��ڿ�-HBe������ALTˮƽҲ���������w��HBV���ƻ��S��
��ALTˮƽ���_����Ҫ�������ί��Č����@�N�������ԑ���IFN�ί��Ěvʷ��������ںY�x�����܌����������A�a������Ļ���Ⱥ�w����ALTˮƽ�����������^��Ҫ��Ч�ί��ļ�����B������HBV��Ⱦ����Ȼʷ���������ί�ԭ�t��������Ҫ�M�п������ί����ߵļ�����B�����綨��Ȼ������M�п������ί��x���mȻ�˽�ߵ�ALTˮƽ�����ڌ����������Д࣬��������ALTˮƽ�������������Q����Щ������Ҫ���ܿ������ί������ߵ�ALTˮƽ��Ҫ�cѪ��HBV DNA�����g�����ؽY�������M�п��]����ˣ�����HBV DNA��104IU/ml��ALT�����Ļ��ߑ����]�M�иλ�z����������Щ���g����35��40�q����Ӌ��̫����̎���������ܠ�B�Ļ��ߡ����λ�z�l�F�����@���ĸ��K�p�����༴�жȣ�2�ڣ����ж����ϸ��w�S���ͣ����@���ĉ������װY�Ļ��ߣ��������ܿ������ί�������HBV DNA��104IU/ml��ALTˮƽ���ߵĻ��ߣ���Փ�Ƿ��M�иλ�z��һ�㑪�o�迹�����ί���
������������HBV DNA���ֵ ���y�ϣ����s�����g�z�yHBV DNA�ĽY���顰��ԣ����^�z�y���ޣ�������ԣ����ڙz�y���ޣ������Д�����ί��������Ҫ�Q�����ء��@������ڴ�����ѽ��l��HBeAgѪ��W�D�Q�Ļ��ߣ���HBV DNAˮƽ�����ǔU���Ԝy�����ęz�y���ޣ���105��ؐ/ml����ALTˮƽ�֏��������������װY�p�p��CHB���ߵ�HBV DNAˮƽ���в����ԣ��Еr���ܕ������@�N�z�y���ޡ����⣬�c�β��Mչ���P��HBV DNA�ֵĿǰ��������������J�飬���s�����g���ܜy����HBV DNAˮƽ���R���ϛ]���@�������x��������20 000 IU/ml��Ѫ��HBV DNAˮƽ�c���@����HBV DNA�����r�]�ϭh��DNA(cccDNA��ˮƽ�����P�ġ����ߣ����ڑ����s�������ܜy����Ӳ����HCC���ߵ�HBV DNA����HBsAg�z�y�Y��Ҳ����ԣ����F����PCR��������Ѫ�弰���K�Мy��HBV DNA�����еČ��r����U��ԇ����Roche Taqman PCR���������əz�y������10 IU/ml��50��ؐ/ml����HBV DNAˮƽ���mȻ��ˮƽHBV DNA���R�����x�в�����������Y���@ʾHBV DNA��105��ؐ��ml�Ļ����аlչ���Ӳ����HCC��Σ�U��
�S�����еČ��rPCR�������ij��F��Ѫ��HBV DNAˮƽ�ڌ�CHB���ߵ��S�L�u�����ѳɞ�������õĺ����ֶΡ���26��ǰհ���о����Ļ�����l�F�������d��ˮƽ���d����׃���c��N���V�����ܵļ�����Ә�־���M���W�ּ��������W��Ѫ��W�����@�����P�����˴_���Ƿ����һ�������@�����R�����x��HBV DNA�ֵ��Chu�Ȳ���PCR����̎�ڲ�ͬ�����A�ε�165���Ї�������؞�ӱ���HBV DNA�M���˷��������l�Ի�IFN�ί���l��HBeAg����Ļ��ߣ�Ѫ��HBV DNA�d��ƽ���½���3 log10�������]��ijһ�NHBV DNA�ֵ�cHBeAg����ʧ���P�����ң�HBeAg��ʧ�r��Ѫ��HBV DNA�d������������HBeAg��ʧ�־��Ե��A�yָ�ˡ�HBeAg��+�������^HBeAg��-�����߃A���ړ����^��ˮƽ��HBV DNA (105һ108��ؐ/ml)������ijЩHBeAg(-)����Ҳ�y���˸��_108��ؐ/ml��HBV DNA�����ߣ���s1/3��HBeAg��-�����ߵ�HBV DNAˮƽ���m���^105��ؐ/ml����˼���ǣ�2/3��HBeAg��-�����ߺ͎����еķǻ���Ԕy���ߵ�HBV DNAˮƽ�����mС��105��ؐ��ml����ʾ�����ܴ_��һ��HBV DNA�R��ֵ��cut-off value����^�ַǻ���Ԕy���ߺ�HBeAg��-����CHB���ߡ����͜y��HBV DNA��ALTˮƽ��λ�z�Y�������ڌ��@Щ�����M�Ѕ^�֣��mȻ�λ�z�������á�����һ��о��У�Manesis�Ȉ���������еĶ���PCR���y�õIJ����d��30000��ؐ/ml�Dž^��HBeAg��-��CHB�ͷǻ����HBsAg�y����B�ĺ��mHBV DNAˮƽ���b��HBeAg��-��CHB��HBV DNAˮƽ���в����ԣ�����߀���h��ALTˮƽ������Ѫ��HBV DNA��ˮƽ�Ļ����ڶ����r�g�c�M�ЄӑB�O�y���ԅ^�־������ڷǻ���Ԕy����߀��HBeAg��-��CHB��
�������CHB̎��������ʹ�����еČ��rPCR�������ʴ_�Ļ���HBV DNAˮƽ��Ȼ���ڿ������ί��^�����^�m�������еķ����O�y��ʴ_���ί������Լ��c��ˎ���P�IJ����W������rebound�������÷�PCR���п��ܙz�y�����@���IJ������ƣ��Լ����Н����к����R���������Փ�����ί�ǰ߀���ί��С�
���������߷NȺ �ځ��^���������HBV��Ⱦ���ԇ��a�ڂ������@Щ����HBeAg���m���ڵĕr�g�^�L�����������A�Σ���ALTˮƽ���A����������Ѫ��HBV DNAˮƽ���Ժܸߡ��^������@���ֱ��30��40���Űl��HBeAg�����Ѫ��W�D�Q�����^�m�ʬFHBeAg��+���Ļ��ߣ�Ҫô��Ȼ̎���������ܠ�B��Ҫô���Ժ�lչ�������������l�_����ģʽ��Western pattern of hepatitis�������FALTˮƽ�ij��m���gЪ�����ߡ���ʹ�dz��FHBeAg����Ļ��ߣ�Ҳ���аlչ��HBeAg��-��CHB�ĸ߶��L
�U�����߲�����ء�
�����߃A�����ڸ�ȾHBV��60һ70��l��CHB����Ҫ���l�Y����HCC���ҳ����ڳ��FHBeAgѪ��W�D�Q֮���mȻALT���ߵā����ߌ�IFN�����đ����r�c�����˷N���ƣ�����ǰ�S�������ߵ�ALTˮƽ��������ˌ��������ί��đ������^�͡��ځ����ߣ�IFN�O���ܳ־�����w�ȵ�HBV���½���һ�M�Ї�������IFN�ί�����S�L�о��@ʾ����ʹ����HBeAgѪ��W�D�Q֮����PCR��������91���Ļ����w�șz�y��HBV DNA�����ң��@Щ���߸�Ӳ����HCC�İl������Ȼ�ܸߡ����֮�£��ڸ����˷N��IFN�����HBeAg��߀������HBsAg�������������^�õ��R���ʹ��Y����
�����ĵڶ��NѪ��WģʽҊ�ڷ��ޡ����к����Ҽ���������˹���ݡ��@Щ�^��HBV����ģʽڅ��郺ͯ�ڵġ���һ�ˡ��������S��HBeAg��+���ă�ͯ����ALT���ߣ�HBeAg��Ѫ��W�D�Qڅ�����ڴ��g��ͯ��ʮ�ךq�r�l�����@���Ⱥ��HBV��Ⱦ��Ȼʷ���ځ�����Ⱥ��������Ⱥ֮�g�������ĵ����NģʽҊ�������l�_���ң�Ҳ���@��ͬ�ځ�����Ⱥ�е�ģʽ��HBV��Ⱦ�ڳ����ګ@�ã������Ա�¶���o�}��ע�䶾Ʒ��ݔѪ��������HBV��Ⱦ�����Ի��L�U���@�����Ⱥ�w������͵ģ�С��5�����������ҵ�CHB����څ����F��ALT��HBV DNAˮƽ�^�ߣ��ڿ��w�ό��������ί��đ����^�á�
�ˡ��ί�Ŀ��
CHB�ί���Ŀ����������@������HBV���ƣ���ֹ�β��Mչ���Ӳ��������Ӳ���Ɍ��¸ι���˥�ߺ�HCC������K��������������Ҫ�M�и���ֲ����ˣ��ί�����ҪĿ���ǽ��ͻ�S��HBV DNA�����ˮƽ�������m����HBV DNA���ƣ������@�����l�����ί�Ŀ�ˣ������νM���W�ĸ��ƺ�ALT�������������ί�ǰHBeAg��+��������������һ���ί�Ŀ�ˣ���HBeAg��ʧ��Ѫ��W�D�Q�鿹-HBe,�������ί���ϣ���ģ������ȫ��HBeAgѪ��W�D�Q��ʾ����ֹͣ�������ί���������ͣˎ���^�m�S�֯�Ч�Ŀ����Ժܴ��mȻHBsAg��ʧ��ʮ�������Ŀ�ˣ������ڵĿ������ί����y�_���@�NЧ������˲������鳣�õĿ�����ָ�ˡ�
�š������������ί�HBV��Ⱦ��ˎ��
��1992һ2005�꣬�������������ί�����HBV��Ⱦ��ˎ�������IFN��-2b���������¸��f�����濨�f��PEG- IFN��-2 a��IFN��-2b���ί������ѱ�PEG-IFN��-2aȡ������˱��ί����]��Ҋ�в��ٰ����@�N�x��Ŀǰ���N�µĿ�����ˎ��������{���ί���̎�ڿ����У�����δ�M���R���̘I�����ã������ӑՓ��
ʮ��CHB���ί�����
��һ��HBeAg��+������ ���¸��f�����濨�f��IFN��-2b������PEG -IFN��-2a����������HBeAg��+��������HBV��Ⱦ�ߵ�һ���������ί���
1����Ҫ�R���Y�ϸ���
��1�����¸��f�� ���ð��¸��f10 mg���ڷ���ÿ��1�Σ��B�m1�꣬�νM���W�@�ø��ƣ�Ѫ��HBV DNA��ALTˮƽ�½���HBeAgѪ��W�D�Q�����ӣ�Ҋ��4�����ί����^48�ܵĻ��߫@�����Mһ���IJ����W��Ѫ��W���R��Ч�档�ڷ�ˎ��144�ܣ�53%�Ļ��߳��FHBeAg��ʧ��46%�Ļ��߳��FHBeAgѪ��W�D�Q��48%�Ļ��߲��ܜy��HBV DNA��80����ALT�������½�����HBeAg��-�����ߵ��S�C�����ա�ǰհ������о���һ��_�Ř�ӛ(open-label)����ԇ�ij�������@ʾ���L�ڑ��ð��¸��f�ί�4��5���ʹ���w�S�����m���ơ����ί�4���5���ALTˮƽ�����߷քe��70%��69%��HBV DNAˮƽС��3log10��ؐ�߷քe��65%��67%��6����5%������HBsAg��ʧ������5�����߳��F��-HBs���@Щ����Ҳ���F���m�ĸνM���W���ơ����¸��f�İ�ȫ���c��ο�����ơ���10mg�ί��M���]�л��߳��FѪ�弡���ߡ�0.5mg/dl���M�ܼ����߿�Ҋ���^�߄����İ��¸��f�ί�����30mg�ί��M��8%�Ļ��߳��FѪ�弡�����ߣ����mȻ��ȱ��1�����ϵı��^�Y�ϣ���Ѫ�弡ˮƽ�����İl�����ڵ�1��o���@��e���I���ԃHҊ��ˎ�������аl�A��ʹ���^�߄����İ��¸��f�r���c������ȣ����¸��f���ί�1��rδ�l�F��ˎ���P׃�����½���4��5���S�L�о�����ˎ�O�y�Y���@ʾ�����¸��f�ί��ڵ�2��3��4��5����F��ˎ׃����N236T��A181V/T�Ļ��߰ٷ��ʷքe��3%��11%��18%��29%�����¸��f�ί�48�ܺ���FHBV DNAˮƽ���ߵĻ��ߣ��l����ˎ���L�U��ߡ��w��ԇ��@ʾ��N236T׃�������Ͷ��w���f��Ȼ���С�Ȼ����A181V׃�������Ͷ��濨�f���������½����������Z���f��tenofovir�������С��о��@ʾ������Ѫ��HBV DNA��ALTˮƽ�����İ��¸��f��ˎ�������ί��Կɮa���������ڰ��¸��f��ˎ�������R���K�c��Ӱ푣�Ŀǰ��ȱ�������Y�ϡ�
��2�����濨�f �c��������100mg/d��ȣ����濨�f��0.5mg/d��48�ܕr���@�õĽM���W�����ʸ��ߣ�72%��62%����HBV DNA�½��̶ȸ�����-6.9��-5.4log10����HBV DNA<300��ؐ/ml�Ļ��߸���(67%��36%)��ALT��1��ULN�߸���Ҋ��68%��60%�����mȻ���濨�f��Ŀǰ����Ѫ��HBV DNAЧ�����Ŀڷ�ˎ�����ί�1����Y���@ʾ���䌦HBeAg��ʧ��Ѫ��W�D�Q��Ӱ��c������Ȳ�o�@���ԣ�Ҋ��4�������濨�f����48�����ϵİ�ȫ�����c�c�������ơ�
�½�һ헳���������������ί�48�ܺ�H�@�ò����W���𣬼��H���FHBV DNA<0.7Meq/ml��HBeAg����ԵĻ��ߣ��^�m�o����濨�f�������ί���2����ܜy��Ѫ��HBV DNA�Ļ��߱������濨�f�M�@���������M��80%��39%��P<0.0001�������濨�f�M��HBeAgѪ��W�D�Q���ƺ�Ҳ�������M��31%��25%������o�@���ԣ�����Փ���ί�48��߀��96�ܣ����濨�f�M��δ�l�FHBV DNA�ۺ�ø׃�������濨�f�ĸ�Ч���ʺ��ί�2���ԟo��ˎ׃�����ɞ�CHB�������ί���һ���O���x��
��3���ɔ_�� ��15�ԇ���C�ͷ����@ʾ��IFN�ί��ɴ��MHBeAg��ʧ��HBeAgѪ��W�D�Q��Ҋ��4����ALTˮƽ���ߺ͵�ˮƽѪ��HBV DNA�nj��ɔ_���ί��a�����������A�yָ�ˡ��S����������HBV��Ⱦ��ALT�����������ڸ�ˮƽHBV DNA�rҲ����ˣ���ˌ�IFN�đ���ܲ�ښW���о����^�쵽�_ʼIFN�ί���1�����5��һ10%�Ļ���HBsAg��ʧ���ڮa�����m����Ļ����У��@һ�����ڵ�5������11%��25%�����ځ�������δ���^�쵽�@�N�о��Y����IFN��ҪƤ��ע�䣬���ί��^���пɳ��F��N�����������������ИӰY�ƣ�ڡ���ʳ�������������p�ٵȡ������x����IFN����A���ί������Ļ��ߣ�PEG-IFN���п���ȡ���˜�IFN��ʹ�á�
��4������ ���������ί�1��ɫ@�ýM���W���ơ�HBeAgѪ��W�D�Q��HBV DNA���Ƽ�ALT�ͳ���Ҋ��4���������HBeAgѪ��W�D�Q֮ǰ��ֹͣ�ί��������³��F�������ơ���ˣ��S�����Ҫ�M���L���ί���HBeAg��Ѫ��W�D�Q���S�����Õr�g�����L����ߣ����ί�1��r��17����������2��3��4��5��r��27%��40%��47%��50%��HBeAg��Ѫ��W�D�Q��߀�S�ί�ǰALTˮƽ�����߶����ߡ���4�����ԇ�ķ����@ʾ���ί�ǰALT��5��ULN��56%���߳��FHBeAg��ʧ�����ҵ��ǣ�������ˎ���S�ί��r�g�����L�����ӣ��ɵ�1��r��14%��������5��r��69%���l��������ˎ�Ļ��ߣ���HBV DNA��ALTˮƽڅ�����ί�ǰ��ˮƽ������������Y���@ʾ��ijЩ���ߵij����νM���W���ƿɳ��F���D�����ң���ijЩ���ߣ�������ˎ����ij��F�c���ص�ALT
������flares�������cѸ�ٵĸι���ʧ�������P�����ߌ��������������ã���ȫ��Ҳ�O�ѡ�
��5��PEG-IFN��-2a ��Փ�Ƿ��c�����ã�����PEG-IFN��-2a�ί�48�����@�õ�HBeAgѪ��W�D�Q�ʡ�HBV DNA��D�ʼ�ALT�ďͳ��ʾ��@�����چΪ����������ί��r��Ҋ��4)���ί���24�ܕr��HBeAgѪ��W�D�Q�ʣ��چΪ�����PEG-IFN��-2a�M��PEG- IFN��-2a���������ί��M���Ϊ��������M�քe��32%��27%��19%���mȻPEG-IFN��-2a���������ί��ܫ@�ø��@���IJ����d���½���������HBeAg��Ѫ��W�D�Q�ʶ��ԣ����ί��ƺ������ȆΪ�����PEG-IFN��-2a��Խ���^�ߵ�HBeAgѪ��W�D�Q��Ҋ��HBV�������r�¡��mȻ���PEG-IFN��-2a�IJ����������@�����������䰲ȫ�����@������ͨ�ɔ_�ء�
��6�����ί� һЩԇ���ʾ������IFN���ί��ɫ@��ijЩ���Ч���������������OӋ�Ĵ�ӱ��о����C���@Щ�����^��Y�����½���HBeAg��-����HBeAg��+���������M�е��о��@ʾ���ϑ���PEG-IFN��-2a�������c�Ϊ�����PEG-IFN��-2a�ί�1�����^���o������á�һ�С���pä�������о�������30�������S�C���ܰ��¸��f�¸��f�Ӷ������I�ί���48�ܺ����ί��MHBV DNA�����Ƴ̶��@�����ڰ��¸��f�Ϊ��ί��M��5. 44 log10��3.40��ؐ/ml����Ȼ��������һ����Ƶ��о��У��������Ͱ��¸��f���ί������ȆΪ���������Ч�á����ί����A����ˎ������ܸ���Ч�������������OӋ�Ĵ�ӱ��R��ԇ���C����
��7������ij־��� 4һ8����S�L�u���@ʾ��80%һ90%�Ļ�����IFN�ί�����T���־õ�HBeAg��ʧ�����P�����ί���־��Ե��Y�����ޡ�һ헌������ί����g���FHBeAgѪ��W�D�Q���ߵ��S�L�о��@ʾ��ƽ���S�L37���£�5һ46���£������ܱ���Ѫ��W�D�Q�Ļ��ߞ�77%��30/39�����^������R���t���J�飬HBeAg��Ѫ��W�D�Q���چμ���HBeAg��ʧ����Ŀǰ�Բ��ܴ_���������ί�����ij־����Ƿ����@�N��e��Ӱ푡������T����HBeAgѪ��W�D�Q�ij־��Կ����ܵ�HBeAgѪ��W�D�Q���^�m�ί�����Ӱ푡����n����һ��о��У�HBeAgѪ��W�D�Q���^�m������������4���µĻ��ߣ��^֮�H�^�m����2���µĻ��ߣ���2��Ͱl���^�ͣ�32%��74%�����@Щ�Y��֧���ڳ��FHBeAgѪ��W�D�Q���^�m������������6���¡��½�һ헌�61��Ѫ��HBeAg��HBV DNA����Һ�s���������m��ԵĻ������ّ��������ί�24���£����������ί���Ѫ��HBV DNA���۷e�ͬF����6���¡�1���2��r�քe��15����21����31����Ѫ��HBeAg���۷e�ͬF�ʷքe��11��,13%��16%����ʾ�����L�����ί�������HBeAgѪ��W�D�Q�ij־��ԡ�
��һ�M���¸��f�ί��Y���Ļ���ƽ���S�L�^��55�ܣ��@ʾ���¸��f�ί���@�ó־�HBeAgѪ��W�D�Q�Ļ��ߞ�91%���־ñ���HBeAgѪ��W�D�Q�Ļ��ߣ��^δ�ܳ־ñ���HBeAgѪ��W�D�Q�ߵ��D�Q���^�m�ί��r�g���L��48�܌�23�ܣ������濨�f�ί��Y�����24�ܣ��־ñ���HBeAgѪ��W�D�Q�Ļ��ߞ�82%����֮���ڽY���������ί����S�L6���r���־ñ���HBeAgѪ��W�D�Q�Ļ�����INF��-2b��80%һ90%��������50%һ80%���ڰ��¸��f��91�����ڶ��濨�f��82����
(8)�ί�������A�yָ�� һϵ���R����������Ѫ��Wָ�˱������Д���IFN�����Ñ�����A�yָ�ˡ�Ȼ������õ��A�yָ����ALT��HBV DNAˮƽ���@Щ����߀�c�^�ߵ��l��HBeAgѪ��W�D�Q�����P���½����о��@ʾ��HBV�����Ϳ���Ӱ푌�IFN�đ����ί�ǰALTˮƽ�^��Ҳ���A�y�����Ͱ��¸��f�ί������Ñ�������ָ�ˡ�
2�������h��HBeAg����������
��HBeAg���������ߵ��ί����]��Ҋ���Y�ڱ�5������С�M���]��Ѫ��HBV DNA��20 000 IU/ml����HBeAg���������ߺ������ί��ֵ����HBV DNA��20 000 IU/ml�Ļ��ߣ������]��Ҏ�M�п������ί�����������@��ߌ��ڷǻ����HBsAg �y���ߣ��β��l�����L�U�^�͡����ڴ��ڼ����������W���M���W���R���Mչ���L�U����ˑ��������е�HBV DNA�z�y�����M�зe�O�ıO�ء����������ߵľ��w��r����A����Ҫ�r���M�иλ�z�����ڰl�F���@���ĸβ��M���W�C���r���]�o���ί��������ί��Ļ��ߑ��ڳ���1��ÿ3���±O�y1�Σ��Ա��CHBV DNA��ALTˮƽ�_��̎�ڷ�����B�������O�y����Ȼ�������t���Ժ�ÿ6-12���±O�y1�Ρ�
a��������λ��IU/ml��1 IU/ml�s����5 .6��ؐ/ml)
b.Ѫ��ALT��ȵ���������������30 IU/L��Ů��19 IU/L
c.�ڳ����\�࣬1����ÿ3���z��1�Σ��Դ_��������
d.�z�yHBV�����Ϳ��������ڛQ����ʹ��PEG-IFN��-2a߀�ǰ���
���f����濨�f��PEG-IFN��HBV������A���ί�Ч�����ڻ�
����D)
e�������x��PEG-IFN��-2a�Ͷ��濨�f��������������S�C�R
��ԇ��@ʾǰ���߯�Ч�����^�ã������đ���߀�ܵ���
��ˎ�ʵ�����
��Ѫ��HBV DNA��20 000 IU/ml��HBeAg��+�����ߣ�������ALTˮƽ�Q���Ƿ�o���ί���ALTˮƽ������ALTˮƽ���ߵĻ��߳��F�������ƵĎ��ʽӽ�����ǰ�߳��FHBeAg��ʧ�Ď����^�͡�����ALTˮƽ�����Ļ���Ҳ���Դ����@���ĸνM���W��׃���Ҳ��������c�M���W�������P����ˑ����]���@Щ�����M�иλ�z�������nj����g���^35-40�q�Ļ��ߡ����λ�z�C�����ڸβ����t�����o���ί�����Ѫ��HBV DNA��20 000 IU/ml��ALT�����Ļ��ߣ��俹�����ί�Ч�������Mһ���о�����Ѫ��HBV DNA��20 000 IU/ml��ALT���ߵĻ��ߣ��������¸��f�����濨�f��PEG-IFN��-2a���ɿ��]����һ���x��ˎ�Ȼ��������Ѫ��HBV DNAˮƽ�^�ߺͣ���ALTˮƽ�����Ļ��ߣ����¸��f����濨�f�����郞���x������@��ߌ�IFN�ί��đ����ʵͣ���������ˎ�����^�ߡ��y��HBV�����������ڛQ���Ƿ����PEG-IFN��-2a�M���ί���������Y���@ʾ����ȾHBV������A�Ļ��ߌ��@�N�������ί��đ���Ч���ڸ��N������HBV��Ⱦ������õġ��������S�C�R��ԇ����ѽ��C��PEG-IFN��-2a�Ͷ��濨�f�������������������^�ߵ���ˎ�ʣ���˲����]������������HBeAg���������ߵ�һ����ˎ����ALTˮƽ�����Ļ��ߣ��mȻ�ڷ����գ���������������Ч����Ѫ��HBV DNA���Ķ�����һ�����ί�Ч�������@�N��r�µ�HBeAgѪ��W�D�Q������Ҋ��

��Փ�Ǒ��ö��濨�f߀�ǰ��¸��f�ί������ί����g��������ÿ6���±O�y1�Ρ������������ί�����M��l�F��ˎ�����M�и����еıO�y������Ŀǰ�ɹ��������Y�ϣ�����С�M���h�����ߑ����ί���HBeAgѪ��W�D�Q��HBV DNAˮƽ������PCR�y������Ȼ�����^�m�ί�6һ12���¡����ګ@��HBeAgѪ��W�D�Q�����ܷ����y��HBV DNA�Ļ��ߣ����^�m�ί�6���£����ٴ��C��HBeAg��Ѫ��W�D�Q�ɿ��]ͣˎ�����Ǹ�Ӳ�����ߣ������Ͱl�Ļ��߿��M�����Ρ�HBeAg������������δ�ܫ@��HBeAg��ʧ���t���L���ί������HBeAg��Ѫ��W�D�Q�S�r�g���L�����ӡ�
������HBeAg��-������ HBeAg��-������HBV��Ⱦ�ߵ��ί��K�c�^HBeAg���������߸��y�M���u�������o���\��HBeAgѪ��W�D�Q�@һ����ָ�ˡ���ˣ�HBV DNA�����ƺ�ALTˮƽ�ďͳ����R����Ψһ���õ��Д��ί������ָ�ˣ����Ҹ�����Ҫ�M���L���ί��ԾS���@Щ����
1����Ҫ�Y�ϸ���
��1�����¸��f�� ���¸��f�ί�1�꣬64%�Ļ��߿ɫ@�ýM���W���ƣ�Ѫ��HBV DNAˮƽƽ���½�3.91log10��ؐ/ml����ο���M��33%���H�½�1.35 log10��ؐ/ml����51%�Ļ��߳��FѪ��HBV DNA<400��ؐ/ml����ο���M�o1�����F����72%�Ļ��߳��FALT��������ο���M�H��29%�����½����Y���@ʾ�����¸��f�ί�144�ܿɫ@���L�ڲ����W�������W���ơ��ڵ�144�ܣ�79%�Ļ���Ѫ��HBV DNA<1000��ؐ/ml��69%�Ļ���ALT�֏�������һС���ֻ����ڵ�144�ܕrͬ����ܸ��Ӹλ�z���Y���@ʾ���Mһ���ĸνM���W���ơ����⣬4���5����Y��Ҳ�@ʾ�г��m�ĸνM���W���ơ����ߌ����¸��f�����������ã����¸��f�İ�ȫ���c��ο�����ơ�4�����ߣ�3%�����C������Ѫ�弡�����ߡ�0.5mg/dL���ί��M48�ܕrδ�^�쵽���¸��f��ˎ׃�������S���^�쵽���¸��f��ˎ׃��N236T��
��2�����濨�f �Զ��濨�f�ί�48�ܣ��c������ȣ��@���˸����@���ĽM���W�����ʣ�70%��61������HBV DNA�½����ȣ�-5.0��һ4. 5 log10����HBV DNA < 300��ؐ��ml�Ļ��ߔ�(90%��72%�����ί����ܙz�y��HBV DNA�Ļ��߱����ܸߣ��@ʾ�˶��濨�f��������Ʋ��������������濨�f�ί��MALT�ͳ�����1��ULN�����@�����������սM��78%��71���������ڸ��w�S���ĸ��Ʒ�����߲�o�@���ԡ����濨�f�ί�48�����ϵİ�ȫ�����c�c�������ơ��ڵ�48�ܺ�96�ܾ�δ�l�FHBV DNA�ۺ�ø�аl�����濨�f��ˎ׃����
��3����ͨ�ɔ_�� IFN�ί�HBeAg��һ�����߽Y���r�đ�����40��һ90%���ȣ����Ͱl�ʅs���_30%һ90%�����w�ϣ����m�����W�����ʼs��15��һ25�����ί�12���µĻ��ߑ����������־ã�����32%�@�ó־ò����W����Ļ��߿��^�m�l��HBsAg�����������IFN�ί����@�ó־ò����W����Ļ��ߣ�������͟o���l�Y��r���@�����ڟo������δ�ί��ߡ�
��4������ ���w�ϣ������ί�6-12���º��s2/3�Ļ��߿ɳ��F�����W�Ͳ����W���𣬸νM���������װY�ĸ�����Ҳ������ˡ����ǣ�һ��ֹͣ�ί����^��������ߕ��Ͱl���Ҵ�������������ڰl��������ˎ���Ͱl��Ȼ�����½�һ��о���ʾ��Ѫ��HBV DNA���m���ܙz���Ļ��ߣ�2����ͣ�������ҏͰl�ʵ����������о���������@Щ�Y�������Mһ���C���������L���ί��ɾS��������ALTˮƽ�͙z�y����HBV DNA�����ڰl����������ˎ��YMDD׃���ɰl�������W�Ͳ����W�ķ�����һ��L�������ί��о��@ʾ���mȻ�ί�12���rALT��HBV DNA�đ����ʷքe��96����68%�����˺����S�ί��r�g�����L�����½����ί�30�������ϕr���H�s40%�Ļ��߾S��������ALTˮƽ�Ͳ��ܙz�y��HBV DNA��������ˎ�İl�����S��ˎ�r�g�����L�����ӣ���1��l��YMDD׃���Ļ��ߞ�19%һ27%����2������44%����4����_60%���@��FYMDD׃�������Ⱥ�����R���Ͽɳ��F�@���ĸ��ף�����@������������HBeAg��һ������HBV��Ⱦ�ߵ��ί����á�
��5��PEG-IFN��-2a ����PEG IFN��-2a�ί�48�ܣ��c���c�����ã����ί��Y����24���@ʾ�˸��@����ALT�ͳ��ʣ������Ѫ��z�y����HBV DNA����400��ؐ/ml).ͣˎ��24�ܕr���� PEG-IFN��-2a�Ϊ��ί��M��ALT�ͳ��͙z�y����HBV DNA�ı����քe��59%��19%����PEG-IFN��-2a/�������ί��M���քe��60����20%�������Ϊ��ί��M���քe��44����7����PEG-IFN��-2a/��������ˎδ���@ʾ�ȆΪ�����PEG-IFN��-2a���õă��ݡ�HBsAg��Ѫ��W�D�Q���چΪ�����PEG-IFN��-2a�M��PEG- IFNa-2a/�������ί��M�͆Ϊ��������M�քe��3%��2%��0%��������ˎ����F�Ď��ʣ����ί��M���@�������Ϊ��ί��M���M�܈��PEG-IFN��-2a�ί��M�IJ����������@���������ί��M�����䰲ȫ�����c�^֮��ҎIFN�����˝M��ġ�
2�������h��HBeAg��-������
��HBeAg��һ�����ߵ��ί����]Ҋ��6��Chu�Ȉ�����ھ��\�r�ij��ڙz�y�У���s1/2��HBeAg��һ�����ߵ�HBV DNAˮƽ���m����105��ؐ/ml������HBeAg��һ�����ߵ�Ѫ��HBV DNAˮƽڅ���^HBeAg���������ߞ�ͣ����Կɴ��ڸβ�����ˌ��ҽM���h��HBV DNA �� 2 000 IU/ml��HBeAg��һ�������M���ί������������h�c��HBeAg���������ߵ����]��Ҋ���ơ����¸��f�����濨�f��PEG-IFN��-2a��������һ���x�����ڽ^�����������Ҫ�L���ί������ǰl��HBsAgѪ��W�D�Q�����@һ�㲻���ܣ�����˲����]ʹ���������������ˎ�L�U�^�ߡ�

a��������λ��IU/ml��1 IU/ml�s����5��6��ؐ/ml)
b.Ѫ��ALT��ȵ���������������30 IU/L��Ů��19 IU/L
c.�ڳ����\�࣬1����ÿ3���z��1�Σ��Դ_��������
d.�z�yHBV�����Ϳ��������ڛQ����ʹ��PEG-IFN��-2a߀�ǰ���
���f����濨�f��PEG-IFN��HBV������A���ί�Ч�����ڻ�
����D)
e.�������J���Ǻ������ί��x������L�ڑ�������
�l����ˎ���L�U�ܸߣ������S�C�R��ԇ��@ʾ�䲻��PEG-IFN��-
2a�Ͷ��濨�f
�������ί��Ļ��ߑ���ÿ6���±O�y1�Ρ��mȻ�L���ί�(12���£��^�����ί���4һ6���£���ͣˎ��ij��m�����W���������������IFN�į���Ŀǰ�Բ�ʮ����������ҽM����PEG-IFN��-2a��ȡ���˜�IFN��-2b���c�ڷ�ˎ����ȣ����ߌ�IFN�������Ԇ��}���^ͻ�������濨�f�Ͱ��¸��f��Ҫ�L�ڷ��ã���Ŀǰ��ȱ�����濨�f��ˎ2�����ϵ��L���Y�ϡ��ί����g����ÿ6���±O�y1��HBV DNA(PCR��)��ALTˮƽ��
�������������ί���ˎ�Ļ��� ������S��CHB�ڷ��������ί�ˎ��đ��ó������P����ˎHBV׃������F���ڷ�������ˎ�����ˎ�ʿ��YҊ��7����������ˎ���������A�����Լ����ܵ�̎�����YҊ��8��
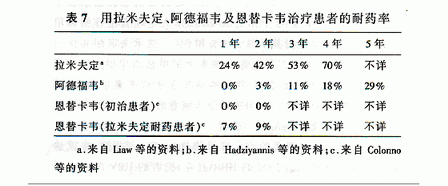
��ˎ�İl���c��ʼ�������ʧ���P�����F��HBV DNA�������S֮ALTˮƽ���ߣ����@�õĽM���W�����S֮Ҳ�l�����D����ijЩ���ߣ�߀�ɳ��F�c���鼱�Լӄ���exacerbations�����P���Mչ�Ըβ���������ˎ�������л��߷NȺ�еõ����������������Ժ�ʧ�����Ըβ����ߡ�������ֲ�����Լ�����HBV/HIV�ϲ���Ⱦ�Ļ��ߡ���Ӳ��������ˎ�İl���cALTˮƽ�����ߣ����ܺ܇��أ������K�ϳɹ��ܵĜp�����P���Ķ�����ʧ�����Ըβ���������ˎ���A�yָ�˰������ί�ǰHBV DNAˮƽ�^�ߡ��ǁ����˷N�����Ի��ߺ�BMI�����_ʼ�ί���@��HBV DNAˮƽ���ߣ��������R���Ͽɜʴ_�\���������ˎ���@�NHBV DNAˮƽ�ĵ��������c���K�p�����P��Ѫ��ALTˮƽ���ߣ����@�N�R����ˎ�\���cHBV�ۺ�ø׃���Ļ����͘�־�������P���]�б�Ҫͨ�^HBV DNAֱ�Ӝy����C����ˎ�İl����
�ڰ��¸��f�ί�48�����ϵ�HBeAg��+����HBeAg��-�������о��^�쵽�����¸��f����ˎ׃����һЩ�Y����ʾ���ϑ������Ͱ��¸��f�M���ί��Ļ��߲����F���¸��f���P����ˎ׃����������ˎ�l����Ҳ�^�͡���δʹ���^����������M���ί��Ļ��ߣ����ö��濨�f�ί�96��δ�l�F��ˎ�������ѽ�����YMDD׃��������������ˎ�Ļ��ߣ������^�쵽�����濨�f����ˎ��Ҋ��7����
1����Ҫ�R���Y�ϸ�������������ˎ��HBV
��1�����¸��f�� �Д���о������¸��f�ί�������ˎHBV��Ч���M�����u�r��һ��о��u�r�ˆ��ð��¸��f��������������ˎHBV�Ī����ί�Ч�����c�^�mʹ�������ܽ���HBV DNAˮƽ��ȣ����ð��¸��f�¸��f/������ʹ�þ�������Ѫ��HBV DNA�ҳ̶�������ڏ������D�Q�����ð��¸��f�ί����g���]�л��߳��F�R�����@����ALTˮƽ���ߡ����ί��r���ߵ����������á��½�����о���ʾ��������ˎ�Ļ����ڏ������D�Q�鰢�¸��f�ί����F���¸��f��ˎ׃���Ď��ʸ��ڳ�ʼ�������ί���ʹ�ð��¸��f�Ļ��ߣ��ί�2��r����ˎ׃���ʷքe��15%��19%��3%�����½���һ��о��@ʾ����ǰ���ܻ�δ�����^�����ί��Ļ��ߣ����¸��f��������ʹ��Ҫ�Ȇ��ð��¸��f�ί��ɫ@�ø������־õ�HBV DNAˮƽ�����ƣ�6.2log10��4.2log10����������HBV DNA�z�y�����ߵı����ڃɽM֮�g����������W�ͽM���W����Ҳ������@Щ�о��@ʾ���������]���ί��A���Ժ�l��������ˎ�����D�Q����ܰ��¸��f�ί����Mչ�Ըβ����ߣ����]���c���¸��f��ˎ���P���R��������ڸ�Ӳ���������^�mʹ�����Ӱ��¸��f�Ŀ��ܸ�����Щ��
��2�����濨�f һ��о���HBeAg��+����������ˎ���ߑ����^�߄����Ķ��濨�f��1.0mg/d���M���ί������c���m��������100mg/d�M�Ќ��ա��Y���@ʾ�����濨�f�M�@�õĽM���W�����ʣ�55%��28%����HBV DNA���͵ķ��ȣ�-5.14��-0.48log10����HBV DNA<400��ؐ/ml�Ļ��߱�����21%��1%����HBeAg����ʧ�ʣ�10%��3������ALT��1.25��ULN�ďͳ���(75%��23%�������ڌ��սM��Ȼ������������ָ�˵ĽK�c�����c��ʼ�������ί���ֱ��ʹ�ö��濨�f�Ļ�����Ⱦ��^�͡����⣬������ˎ�����ί�1���7���Ļ��߳��F�µ���ˎ׃����1.6%�Ļ��߳��F�˷�����Ѫ��HBV DNAˮƽ���ߡ�2����S�L�u���@ʾ��9%�Ļ��߳��F��ˎ���l�������W������Ҋ��7����

2���ί����h����������ˎ��HBV����
�l��HBV��ˎ���ߵ�̎���x�YҊ��8����������ˎ�Ļ��ߣ����¸��f�Ͷ��濨�f���ǿ��Խ��ܵ��x��Ȼ��������Ŀǰ���Y�ϣ���̎��������ˎ��HBV�����¸��f���܃��ڶ��濨�f�������Dz��ð��¸��f�Ϊ��ί���߀�ǰ��¸��f�c�������ί���ȡ�Q�ڻ��ߵĸβ���B��ʧ�����Ըβ����ߵ��Y���@ʾ����������D�Q�鰢�¸��f�ί���ijЩ���߿ɳ��FALTˮƽ�p�����ߣ������o���߳��F�R�����@����ALT���ߡ��@Щ�^��Y����ʾ���S��ߏ������D�Q�鰢�¸��f�ί���һ����ȫ�IJ��ԡ�����Mչ�Ըβ��Ļ��ߣ���HBV׃����؏͞�HBVҰ���꣬�t���Н��ڵĸ�����صĞ��y�Ժ�������D�Q�鰢�¸��f�ί����t��2����¸��f����ˎ�ʸ��_15��һ19������ˣ�����������ˎ�ĸ�Ӳ�����ߣ������^�mʹ�����Ļ��A�ϼ��ð��¸��f�M���ί����P���M���е��о������Y�ό����Ժ�ҕԡ���������������ˎ���ߣ����^�mʹ�����Ļ��A�ϼ��ð��¸��f�����܃����D�Q�鰢�¸��f�Ϊ��ί������濨�f��ʹ������ˎ���ߵ�Ѫ��HBV DNAˮƽ�½�5 log10�����@�N�ί�Ч����Y�϶��濨�f�µĻ���׃���M�Й�⣬��錦������ˎ�Ļ����ڸ��ö��濨�f�ί�1���2��r����ˎ�ʷքe��7%��9%��δ���ί�������ˎ�Ĵ�ʩ�������������Z���f������ö������I�����Z���f���ί������]�İ��¸��f���̼����ί��ıO�y����Y�ϻ��ߵľ��w��r�M�п��]��һ��أ���������HBeAg���������ߑ��ί���HBeAgѪ��W�D�Q�����ܙz�y��HBV DNA (PCR������Ȼ�����^�m���ί�6���£���Ҋ���ί����h��HBeAg�������Ļ��ߡ�����
3����Ҫ�R���Y�ϸ����������¸��f��ˎ��HBV
Ŀǰ�Пo�u�r���¸��f��ˎ�ί�����ʽ�о������Ԃ����о����R���Y���@ʾ�������F���¸��f��ˎ���Pͻ׃N236T��A181V/T�Ļ��ߑ��������ί����ɫ@�ò����W������һ�����ܵIJ������D�Q����濨�f�ί���ǰ���Ǵ�ǰδ���F�^������ˎ��δ�����ܵ��ί��x���Ǹ��ö������I�����Z���f���ί���Ҋ��8����
���ģ���Ӳ�����ߣ������Kĩ�ڸβ����ߣ�
����Ч�Ŀ������ί��ֶγ��F֮ǰ�������Ը�Ӳ����ʧ�����Ը�Ӳ�����ߵ�5�������ʷքe��84%��14��һ35%�����N�R����������Ѫ��đ�t��ˮƽ�����g�^��ȿ��A�y�����ʡ����⣬�ڴ����Ը�Ӳ��HBeAg��ʧ���ߵ�5�������ʞ�97%����HBeAg�������Ļ��ߞ�72%����ʾ�������ƿɌ��²��������
1����Ҫ�R���Y�ϸ���
��1�����¸��f�� һ헡���Ϣ�ί��о�( compassionate-use
study�������ð��¸��f10 mg/d�ί�CHB�������ʧ�����Ը�Ӳ�����������R����ˎ�C�����M�˵Ⱥ����ֲ��226 ���������ֲ��241�����Ļ��ߡ�����ֲ���ߵ��ڰ��¸��f�ί�144�ܺ�Ѫ��HBV DNA��1 000��ؐ/ml�ߞ�78%��ALTˮƽ�����ߞ�58%������ֲǰ���ߵ��S�L�u���r�g�^�̣����ί�96�ܺ�Ѫ��HBV DNA���ܜy����ռ76%��ALTˮƽ������ռ84%����������߷�ӳ���K�ϳɹ��ܵ�ָ�˵õ����ƣ�Child-Turcotte- Pugh�u�ֱ��ַ������и��ơ�����ֲǰ���ߺ���ֲ�������ί�2���������ʷքe���^80%��90%�����@Щ����Ⱥ�У����¸��f�İ�ȫ�����c�c���߸β����A�κͲ��没һ�¡�Ѫ�弡�����ߡ�0. 5 mg/ dlҊ�ڼs21���Ļ��ߡ�
��һ��P�ڰ������ʧ�����Ըβ�����������ˎHBV��Ⱦ���ߵ��о�Ҳ�@�������ƽY�������^�mʹ�����Ļ��A�ϼ��ð��¸��f���ί�48�ܺ�@�����@����Ѫ��HBV
DNA����Ч��(4һ5 log10��ؐ/ml)��ʧ�����Ըβ����ߵ������W�����ι��ܠ�B�õ��@�����ơ�
��2���ɔ_�� �����R���ϴ���ʧ�����Ը�Ӳ���Ļ��ߣ�IFN�đ�����һ�����}���mȻ������IFN�ί����@ʾ�ˑ��𣬵��ί����g�β�څ�������ڽY���ί����蔵�²��ܻ֏��K�����W�����������⣬IFN�ί����ڰl�����ز��l�Y���L�U���������صļ�����Ⱦ���ӄ�����ʧ�����Ի��ߣ��ι���̎��Child- Turcotte-Pugh A���Ļ����^B��C�������ܫ@�ø��õđ����ʣ��քe��100%��33%��0�������̈́�����IFNҲ�����ڷ�A���ĸ�Ӳ������������Ⱦ����ʾIFN���������ί��@Щ���ߡ�IFN�����ί������Ը�Ӳ�����߿����ǰ�ȫ�ģ��M�����L�ί��аl���ι���ʧ������Σ�U���Пo�S�C�R��ԇPEG-IFN���@Щ����Ⱥ�еđ����M���u�r��
��3������ �ѽ��C���������ί����Ӿ��Mչ�Ը��w�S�����Ӳ�����R���M�̡�һ헴����S�C��ο�������о��@ʾ����ƽ���ί�32���º������ί��M7.8%�Ļ����_�����R���K�c�����ڰ�ο�����սM��17.7%�����⣬�ڜp��HCC�l���ʷ��棬�����ί��MҲ�@�����ڰ�ο�����սM(3.9%��7.4%�����mȻ49%���������ί��Ļ��߳��F��YMDD׃�������c��ο�����սM��ȣ��M������ˎ�İl�����@Щ���߳��F���R�����l�Y�^�١���ˣ����������@����ʧ�����Ը�Ӳ�����ߵ��ί��Y�������������о�Ҳ֧���@һ�YՓ��27���Ǹ���ֲ�Ļ��ߑ��������ί�ƽ��869 d��Ѫ��HBV DNAˮƽѸ���½���ALT�֏����������ֻ��߫@����HBeAg�������Ѫ��������đ�t��ˮƽҲ���Ը��ơ�����һ���Villeneuve����ɵ������о��У��������ί����^9�������ϵĻ������^�쵽����ĸ��ơ�Ѫ��HBV DNAˮƽ�½����춬���ᰱ���D��ø��AST) ��ALT�֏����������ס���Ѫøԭ�r�g��Child- Turcotte- Pugh�u�ֵ�Ҳ���Ը��ơ��@����о�߀�@ʾ���c�vʷ������ȣ������ί��M�Ĵ���ʵ��Ը��ơ�Ȼ���������ί�6-12���º�ɳ��FYMDD׃���꣬�R�����F��HBV DNA��ALTˮƽ�����ߡ���ʧ�����Ը�Ӳ�����ߣ�YMDD׃�����c���K��������ʧ����Ч�ʜp�����P��һЩ��Ӳ�����߲�������YMDD׃���꣬һ�����FYMDD׃�����β�����Ѹ�ِ������@Щ�о�֧����������߀�ж��濨�f���Լ����¸��f������Ч�ί��^�l��HBV��Ⱦ��ʧ�����Ը�Ӳ���������Փ��
Ŀǰ�P�ڶ��濨�f�ί��Mչ�Ըβ����Y�����ޡ�����Է������濨�f�����R��ԇ������P��Ӳ�����ߌ��ί��đ�����r���Y���@ʾ���濨�f�ķ������������ã����ί��K�c�r�ĽM���W���ơ�ALT�ͳ���Ѫ��HBV DNAˮƽ�y������ָ�˾����������ί��M���Пo����PEG-IFN��-2 a�ί��Mչ�Ըβ����Y�ϣ���������ͨIFN�ί��@Щ���ߵĽ����ʾ�����@Щ���ߑ�������ʹ��PEG-IFN��-2a��
2���ί����h����Ӳ������
�P��HBeAg��������HBeAg(-���Ĵ����Ժ�ʧ�����Ը�Ӳ�����ί����hҊ��9�ͱ�10������Ѫ��HBV DNA��2000IU/ml�Ĵ����Ը�Ӳ�����ߣ����x��O�y�����ö��濨�f�¸��f�M���ί�������С�M�J�飬�mȻĿǰ�Пo�Y�ρ�ָ���@һ�x�����@���R���β����M���Ǵ����Ըβ����Ļ��ߣ������@Щˎ���M���ί������еĝ����R�������ˎ�ﶾ���L�U���ί����M������Ҫ������Ѫ��HBV DNA��2 000 IU/ml�Ļ��ߣ����濨�f�¸��f�������һ���x����������į�Ч�����õ��������ѽ��õ��C��������С�M�J�飬�mȻ����IFN���T���β����غ�ʧ����������ʹ�ã���PEG-IFN��-2a�������Ը�Ӳ�����ܾ����ί��rֵ���b����Ҫ�L���ί������濨�f�ͺ����¸��f���������@�����������ˎ���^�ߣ����п�����˶������R��ʧ���������¸��f�c��������ܶ��濨�f����ʹ�ã���Փ�Ͽɜp�ٌ�����ijһˎ����ˎ����ͬ�r�p�ٌ��ɷNˎ����ˎ��
��λ��IU/ml��1IU/ml�s����5.6��ؐ/ml����

a.��λ��IU/ml��1 IU/ml�s����5��6��ؐ/ml)
b.�mȻ�Пo�Y�Ͽɹ���������PEG-IFN��-2a�����Ǹι��ܴ������õ����ڸ�Ӳ�����ί��x��֮һ��c.�������ֻ���濨�f���Ͱ��¸��f���ί�����Փ�Ͼ������õ�Ч��������@����ʹ����ˎ�ʸ��͡�

a.��λ��IU/ml��1 IU/ml�s����5��6��ؐ/ml)
b.Ŀǰ�Пo���濨�f�����P�Y�ϣ�PEG-IFN��-2a����ֹʹ��
c.�������ֻ���濨�f���Ͱ��¸��f���ί�����Փ�Ͼ������õ�Ч��������@����ʹ����ˎ�ʸ��͡�
����ʧ�����Ը�Ӳ�����ߣ���Փ��Ѫ��HBV DNAˮƽ��Σ��������]�o���ί������¸��f�c���������˼�濨�f���ϣ���ֵ�Ó��]��һ��ˎ���ʧ�����Ըβ������M���ί���Ŀ���Ǹ����伲����B������ʹ������K�ĸ���ֲ�������Ƴ������ί��ɽ��ͻ����tˎ����ˎ�İl������ˣ����]ʹ�ð��¸��f�c��������ܶ��濨�f���ϑ�������ʧ�����Ըι��ܵ�һ���ί�ˎ���ʧ�����Ը�Ӳ�����ߑ��ð��¸��f���������¸��f�Ӷ��濨�f���������ί��������u���о���������Ҫ�ͺ����ġ�
���ҽM�J�飬��Ӳ�����ߵ��ί��������L�ڵĺ͟o���ڵġ��mȻ���o�P�ڌ������Ը�Ӳ��������HBeAgѪ��W�D�Q���^�m�ί�������Y�ϣ��������Ї����Y���@ʾ����ʹ�l��HBeAgѪ��W�D�Q��Ҳ��Ȼ�п��ܰlչ��HCC���Mչ�Ըβ����@���������ڳ��m���ڵ�ˮƽ��HBV�ͣ������������°����صĆ��Ӻ͂������M�ܲ��������ܵ�����)���mȻȱ������Ӳ������������Y�ϣ����b�ں���/����������Խ�İ�ȫ�����c���ί��������m������Ѫ��HBV DNA�Dꎺ�HBsAg��ʧ���ί����g����ÿ3���±O�y1�Ρ������ж�N�I���ܓp��Σ�U���صĻ��ߣ����ί�ǰ���ί������бO�y�I������ʮ����Ҫ�ġ�ˎƷ���a�S�ґ����������h�����¸��f�����濨�f������ˎ��Ą����l�������{����
���壩HIV/HBV��HCV/HBV�ϲ���Ⱦ�Ļ���
�������͚W�ޣ��s10%��HIV��Ⱦ�ߺϲ���ȾHBV�����Զ��������̲�������о��Y��[�����������ί�ǰ��Ч�����D䛲����ί���HAART������Y��]�@ʾ��HIV/HBV�ϲ���Ⱦ���c���K���P�IJ����ʼs��ɷN�������ԆΪ���Ⱦ�r��14�����кܸ߱�����HIV��Ի��߽����������Z���f�ͣ��������I�ί������@Щˎ��Ҳ���п�HBV���ԡ�
1����Ҫ�R���Y�ϸ���
��1�����¸��f�� ��HIV/HBV�ϲ���Ⱦ���Ұl��������ˎ�Ļ��ߣ����¸��f10mg/d����Ч�ģ���ˎ��144�ܕr�s64%�Ļ��߳��FHBV DNA�½�5.45log10��ALT�֏��������ڵ�96�ܕr������ԇ�Ļ��ߛ]���κ�һ���l�������¸��f��ˎ��HBV DNA�ۺ�ø׃�������ڰ��¸��f10mg/d�]�п�HIVЧ������˰��¸��f�ĺ�̎���ڲ����Y�x���Ͱ��¸��f�������Z���f��HIV׃���ꡣ��2������Ѫ�弡��ˮƽ���ߡ�0.5mg/dl��ͬ�rѪ��o�C�כ]�����@׃�������Ѫ�弡��ˮƽ���ߵ��Խ�Q�������]�c���¸��f�o�P��
��2�����濨�f �½����о��@ʾ�����濨�f�ί�HIV/HBV�ϲ���Ⱦ��Ч��һ헰�ο�������о��Զ��濨�f�ί�HIV/HBV�ϲ���Ⱦ�Ļ��ߣ���ˎ24�ܕrѪ��HBV DNA�½���3.66log10��
��3������ �����о��@ʾ�����ί�HIV/HBV�ϲ���Ⱦ�Ļ�����Ч����ʹѪ��HBV DNA�@���½����������������á���HIV/HBV�ϲ���Ⱦ�Ļ����������ί�4�����ˎ���_90��������HBV�Ϊ���Ⱦ�ߡ�
(4�����Z���f ����о��ѽ��C�������Z���f����Ч�Ŀ�HIV�Ϳ�HBVˎ�Cooper�ȵ�һ��о��@ʾ�����Z���f�ί���ʹHIV�½�6 log10��ʹHBV�Ի����½�5 logl0�����Ƶ�����һ헌�HIV/HBV�ϲ���Ⱦ���о��@ʾ�����Z���f�ί���24��Ѫ��HBV DNA�½���4 logl0��CD4��Լ����s����80����һ�С�͡��_��һ��ӛ�����S�C�о��Č����������ˎ���ߣ�����һ���ֻ��߸�Ⱦ��HIV�������Z���f�¸��f�ί�48�ܣ��Y���@ʾ�����Z���f�M��Ч�����ڰ��¸��f�M��HBV DNA�d���½������^��-5.5��һ2. 8 log10��ؐ/ml)��HBV DNA�D��ʺܸ�(100%��44%)�����ǣ����Y���@ʾ���Z���f�ί����ܳ��F�I���Ժ���Ѫ�Y��
2���ί����h��HIV/HBV�ϲ���Ⱦ
��HIV/HBV�ϲ���Ⱦ�ߵ��ί�����Ҫ�������ߵĠ�B�M�Ђ��Ի������Z���f�����濨�f�����¸��f������Ч�Ŀ�HBVˎ������濨�f�Ͱ��¸��f�]�п�HIV���ԡ������в���Ҫ��HIV�ί��Ļ��ߣ����濨�f�Ͱ��¸��f��HIV���Ե�ȱ���ṩ����Փ�ϵ��ί����ݣ�������ʹHIV��Ⱦ�߲���Ҫ�ر�¶�����Z���f�����Ϊ��ί��ĉ����£��п��ܓp���Ժ�HIV���ί���������߽��ܿ�HIV�ί������x��������Z���f�����Z���f���������Z���f���������I��HAART�������������ڽ��ܷ�����HIV�ί������Ļ��ߣ��˼��ð��¸��f����濨�f��HBV�ί���������ֱ���D�Q�����Z���f��ԇ�Dͬ�r���w���ɷN������
��HCV/HBV�ϲ���Ⱦ�Ļ������o�}ע�䶾Ʒ�߳��ϲ���Ⱦ��HCV��HBV�������о��@ʾHCV/HBV���ϸ�Ⱦ�ĽY���^֮�����κ�һ�N�����Ϊ���Ⱦ��Ҫ���صöࡣ�^���������������һ�N������Ⱦڅ��ռ���ݣ�����һ�N����څ�����ߡ���HCVռ���ݵļ���������Ѫ���Мy��HCV RNA�����ܜy��HBV DNA����֮����HBVռ���ݣ��t����Ѫ���Мy��HBV DNA�����ܜy��HCV RNA���S��HBV/HCV�ϲ���Ⱦ�Ļ���څ����F��HBeAg��-������ˮƽHBV DNA������HCV��Ⱦռ�����ݡ�
�ί����h��HCV/HBV�ϲ���Ⱦ
���ںϲ���ȾHBV��HCV�Ļ��ߣ�Ŀǰ�Пo�˜ʵ��ί������������ߑ����M���u�����Д��ķN������Ⱦռ���ݣ�Ȼ����˽o���ί�����ˣ��������Ѫ��HBV DNA��104IU/m1�����Ҳ��ܜy��HCV RNA���@�r����ᘌ�HBV�M���ί���Ȼ���������S���څ�ڱ��F���ˮƽHBV DNA���s�ɜy��HCV RNA�����ҽM���h����HCV/HBV�ϲ���Ⱦ�ߣ����ܜy��HCV RNA���и�ˮƽ��HBV DNA���t���ؘʄ�����PEG- IFN�������f�֣��������ί�3���£���HBV DNA�o�����������ߣ��t�ɼ��ö��濨�f�¸��f���½�һ��о��@ʾ������HCV��Ⱦռ���ݶ����ܿ�HCV�ί���HCV/HBV�ϲ���Ⱦ�ߣ��䑪����r�c�H������HCV��Ⱦ�Ļ���һ�ӣ�ֻ���ٔ��������ί��^���г��FHBV��Ⱦ�Ļ��
���������W��
�������HBV���Ƶ��ټ��Ѫ��HBV DNA��ALTˮƽ���ߣ���Ҋ��20%һ50%�����������ƻ����Y������HBsAg�y���ߡ��ڽ^��������������İl����o�Y���ԣ���Ҳ�^�쵽���S���Լӄ������ι���ʧ�����������Ļ��ߡ��nj������о��@ʾ���c�vʷ������ȣ��������M���A�����ί��ɜp��HBV�ټ���Ď��ʡ��c�������P�IJ�����ضȼ������ʡ���һ��о��@ʾ���ڻ���ǰ���_ʼ���������M���ί����^֮�ڻ����^���г��FHBV�����ټ���ı��F��Žo�������ί���ǰ�߰l�����R�������^�١��mȻ�@Щ�о��в��پ����ԣ��������������_ʼ�M�л��������������ί��r��HBsAg�y���ߌ������M���A���Կ����������������S�ֿ������ί��s3���¡�������Ҫ�K���������������ί���HBsAg�y���ߣ������I��ֲ���ߣ��в��ܿ϶��A���Կ������ί������棯Σ�U�ȡ�����֮һ�ǿ��Ԍ��@Щ�����M�бO�y�������F�@����HBV DNA��ALTˮƽ���ߣ��t�_ʼ�������ί����mȻ���¸��f�Ͷ��濨�f���������ˎ�����ֹĿǰ���Y����Ҫ��ע�������������������A�����ί�ͨ���Ƕ����ί������������ˎ�����^���Pע��Ȼ��������ί��ܿ�����Ҫ���^6���£����ҽM���hʹ�ð��¸��f����濨�f��������mȻHBV���ټ����п��ܰl����HBsAg��-�����H�п�-HBc��������ͬ�r���ڿ�-HBc�������Ϳ�-HBs�������Ļ��ߣ����@Щ����HBV���ټ����Dz���Ҋ�ģ��˕r�Ƿ���Ҫ��Ҏ�M���A���Կ������ί��Пo����֧����Ϣ��Ȼ�������ҽM���@һ���}��̎������Ҋ���ڷ��磬��鲿�������ڃH�п�-HBc�������Ļ������^�쵽�����ļӄ������F��y��HBsAg�Լ����ص������W���R����׃����ˣ����@Щ���߿��]�o���A���Կ������ί����Dz��M�����������ҽ��h�x�ÿڷ�ˎ�HBsAg��һ������-HBc�������ͣ���-HBs�������Ļ����M���A�����ί���
���ߣ�����
�������濨�f�Ͱ��¸��f���w��C�ˎƷ����ˣ�������ѭ�˜ʵ�C�ˎƷʹ�ý��h��������DŮ�Ƿ��_ʼ�ͣ����^�m���ÿ������ί���������ĸ�H���r�ĸβ���B�����ܫ@�õĝ������棬���m�����]̥�����ܽ��ܵļ�С�L�U�����ڿ������ί���漰���܃H�����p�β������p�DŮ��������t�������Ժ��ٽo�迹�����ί����ܱ��^֔�����mȻ�������ЋD�Б��õİ�ȫ�Խ���h�h���ڰ��¸��f�Ͷ��濨�f��������ʹ�á����Կ��]������ĩ3���½o���ί����A��HBV�����o���������mȻ���������A��HBV�����o��������һЩ���ڳɹ��Ĉ������Ҳ�Ј����ʾ����ʹ��ʹ�������ί������a�������A�����ӷN�������r�£�HBV���п�����ĸ�H�����o���׃����½�һ��pä����ο�����ա��������R��ԇ144��HBsAg���������ЋD�S�C�֞��������100 mg/d�M�Ͱ�ο�����սM���������32�ܕr�_ʼ�ί���Ȼ���ڋ냺1�q�r�u�r��Ѫ��HBsAg������ʣ����Ћ냺�ڳ����r��ע��HBV��������HBIG���ͽӷNHBV���硣�Y���@ʾ�����������ί���ĸ�H�����ċ냺�l��HBV��Ⱦ�Ď��ʵ��ڰ�ο�����սM��18����39%����������������g��Ҫ�ί�������������HIV��Ⱦ�I���ڋDŮ����r�������Ľ��Լ��½����S�Cԇ�Y�������ҽM���h����������һ��ˎ�Ȼ���������Ҫ������Y�����L���ί����t�ɿ��]�ڮa���D�Q�鰢�¸��f����濨�f�ί����κν����������濨�f�Ͱ��¸��f�ί�������DŮ����������Ե�����ע�Ԇ�λ�M�ЅR��
ʮһ����ˎ�O�y
�R����ˎ��Ŀǰ�R������δ��Ҏʹ�û���y�z�y��ˎ����ָ��2�N�z�y���z�y����Ѫ��HBV DNAˮƽ�^�ί��r���ֵ����1��log10���ϣ�Ҋ��8)��
���������ί��Ļ��ߣ�����ÿ3һ6���±O�y��ˎ��r�����ڰ��¸��f�Ͷ��濨�f����ˎ���@���^�ͣ����ί�1����ÿ6���±O�y��ˎ��r�����Mչ�ڸβ��Ļ��ߣ������M�и����еıO�y����ÿ3���±O�y1�Σ���
ʮ�����YՓ
����HBV��Ⱦ�߿������ί���Ŀ������ֹ�β��Mչ���Ӳ����HCC������HBV����Ӱ�����HBV��Ⱦ�ߵ��R���Y�֣���˿������ί�����ҪĿ���dz־�����Ѫ��HBV DNA��ʹ֮�_���M���ܵ͵�ˮƽ��PCR�ȷ����\���W�����ij��Fʹ���܉�ʴ_�O�y����10 IU/ml��Ѫ��HBV DNAˮƽ����������Á�z�y�����ڿ������ί�ǰ��HBV DNA����ˮƽ�����O�y�������ί������c��ˎ���P�IJ����W������
��HBeAg��������CHB���ߣ��_���������ί�������HBV DNA�ֵ���20 000 IU/ml��ALTˮƽ���ߣ�������ӆ�����������������ͣ��λ�z�C�����ڸ��ס�����ALT�������в���Ѫ�Y�Ļ��ߣ����������w��r��Ҫ�M�иλ�z�顣���@�HBV��Ⱦ����Ҫ�ڌ������Mһ���о������������20��һ25%�Ļ��ߴ����@���ĸ��w�S������HBeAg��һ����CHB���ߺ�ʧ�����Ը�Ӳ�����ߣ��_���������ί�����ȡ�^�͵�HBV DNAˮ�ʡ����ҽM���]���ֵ�քe��HBV DNA��2 000 IU/ml�͡�200IU/ml�� HBeAg��һ����CHB���ߺ�Ӳ��������Ҫ�L�ڿ������ί������¸��f�����濨�f��IFN������PEG-IFN��-2a���ѱ���������CHB���ߵij�ʼ�������ί���Ȼ�������x��һ���ί������r���������]�@5�N�ί����Ը��Եă�ȱ�c����Ҫ���]�Ć��}������Ч����ȫ�ԡ���ˎ����ˎ�������ί��M�õȡ�
���¸��f�ڿ��w���c����Ч�ஔ�����һ��ߵ����������á��䃞�c������ˎ�l���^�t���^�١����濨�f��Ŀǰ��Ŀڷ�������ˎ����S�C�R��ԇ�������F�����������⣬����ǰ��δ�����^�������ί��Ļ����У����濨�fʹ��2��δ�l�F��ˎ�Įa����Ȼ����Ŀǰ��ȱ��2�����ϵ��L�گ�Ч����ˎ�^���Y�ϡ����濨�f�Ͱ��¸��f���ί��M�þ����������mȻIFN��PEG-IFN��-2a�������_�į��̡������־õđ������܉�a������Ļ��ߣ���ȱ����ˎ�������ί����r�������F�����ͨ�^ע��oˎ���������S����������ڮ�ǰ���R�����`�У�PEG IFN��-2a�п���ȡ���˜ʵ�IFN�����Ļ������������ã���ȫ�ԘO�ѣ�Ҳ���^�õį�Ч���������ڰl����ˎ��ʹ���L���ί������ܵ����ơ���ˣ����ҽM�����]����������һ��������ˎ��������ڻ����������^�����M�ж��ڵ��A���Կ������ί�����HBV/HIV�ϲ���Ⱦ�����鿹HIV�ί������ĽM�ɲ��ֻ��ڰl���ι���ʧ�����Ļ����c���¸��f��ʹ�á�������Ҫ�ί����^1�����ϵĻ��ߣ����ܵ�����x����ʹ�ð��¸��f����濨�f������@���ߵ���ˎ�ʺܵ͡�
�����I�������Mһ���о�������ˎ���ܱ��C���^��һ��ˎ�ڲ������Ʒ��������Ч�����Һܿ��ܽ��ͻ����t��ˎ�İl����Ŀǰ�����M�Ўׂ����͵��R���о�����̽ӑ��ʹ��2�N���գ������������ˎ����ϑ���һ�N�ڷ�������ˎ���PEG-IFN�������Ըβ����ߵđ���Ч�����ϑ��ÿڷ�������ˎ�ʧ�����Ը�Ӳ�����ߵ��ί������Ⱦ߃rֵ���M���ϑ��ð��¸��f�������c����ij�Nˎ��@����ί�Ч���ı��^�о����@Ȼ��ʮ�ֱ�Ҫ�ġ�
�N�µĺ��x������ˎ���������I����ȷ������Z���f���µĝ��ڵ��ί�����HBV��Ⱦ��ˎ�Ŀǰ�����M���u�����@Щˎ�������δ������пɔU��鿹HBV�ί��x��
TAG���������������ײ�����Ⱦ̎������ ������������ָ�� ���濨�f ��ȷ�
���PˎƷ

�Wվ�YӍ- ˎ����B |
�B�i�T��ֲ� | �˲���Ƹ |
ϵ�҂� | �Wվ�؈D
�������- ��Ҋ���} | ����ָ�� | ˎ�W���� | ���Ҋ | �Ͷ�V | ���Ʒ��� | ���t��ˎ | ˎ������
���Ʒ����- �[���� | �β��� | �� | ����� | Ƥ�w�Բ��� | �� �� | �L�����߿� | ��Ѫ�ܿ� | ���� | ��������ˎ
ˎƷ����- �[����ˎƷ | �����ˎƷ | �β���ˎƷ | �ۿ�ˎƷ |Ƥ�w�Բ���ˎƷ | ��ˎƷ | �L�����߿�ˎƷ
�ٝ�ˎ���Y�|- ��I���ˠI�I���� | ���WˎƷ��Ϣ�����Y���C
�������- ��Ҋ���} | ����ָ�� | ˎ�W���� | ���Ҋ | �Ͷ�V | ���Ʒ��� | ���t��ˎ | ˎ������
���Ʒ����- �[���� | �β��� | �� | ����� | Ƥ�w�Բ��� | �� �� | �L�����߿� | ��Ѫ�ܿ� | ���� | ��������ˎ
ˎƷ����- �[����ˎƷ | �����ˎƷ | �β���ˎƷ | �ۿ�ˎƷ |Ƥ�w�Բ���ˎƷ | ��ˎƷ | �L�����߿�ˎƷ
�ٝ�ˎ���Y�|- ��I���ˠI�I���� | ���WˎƷ��Ϣ�����Y���C







